Neuroendokrine Stressreaktion
Postoperativ verändert der sogenannte Postaggressionsstoffwechsel den Metabolismus. Neben der lokalen posttraumatischen Reaktion wird intraoperativ eine neuroendokrine Stressreaktion ausgelöst, indem über vegetative Regulationsmechanismen Hormone im Hypothalamus (CRH, TRH), in der Hypophyse (TSH, ACTH), Schilddrüse und Nebenniere freigesetzt werden und zugleich der Sympathikotonus erhöht wird.
Postaggressionsstoffwechsel
Die Stressreaktion induziert eine Katabolie mit Hyperglykämie und negativer Stickstoffbilanz sowie nachfolgender Anabolie.
Rasch werden Katecholamine (Noradrenalin, Adrenalin und auch Dopamin) freigesetzt, um den exogenen Stress zu bewältigen. Ihre Plasmaspiegel sinken bei einer mittelgroßen Operation (z.B. Cholezystektomie) allerdings innerhalb von 24 Stunden auf die ursprünglichen Werte. Die Katecholamine aktivieren die hepatische Glykogenolyse, fördern die Freisetzung glucoplastischer Aminosäuren, stimulieren die Lipolyse und hemmen die Sekretion von Insulin.
Hormonfreisetzung
Gleichzeitig mit dem Sympathikus wird auch die Hypothalamus-Hypophysen-Nebennieren-Achse stimuliert. Das Cortisol steigt nach einigen Stunden an, erreicht seinen höchsten Wert ungefähr nach 12 Stunden und fällt innerhalb von wenigen Tagen wieder ab. Die Glucokortikoide stimulieren die Lipolyse, hemmen die Proteinsynthese, setzen vermehrt Aminosäuren aus der Muskulatur frei und fördern die Gluconeogenese in der Leber und Niere. Sie hemmen wie das Adrenalin die Insulinsekretion und setzen gleichzeitig die Insulinempfindlichkeit im peripheren Gewebe herab. Eine feste Beziehung zwischen der Höhe der Cortisolausschüttung und ihrer metabolischen Wirkung auf den Glucose- und Proteinstoffwechsel scheint aber nicht zu bestehen. Eine ähnlich katabole Wirkung entfaltet das Glucagon. Dieses Hormon stimuliert besonders die Gluconeogenese und Glykogenolyse in den Hepatozyten und fördert ebenfalls die Lipolyse und Proteolyse im peripheren Gewebe.
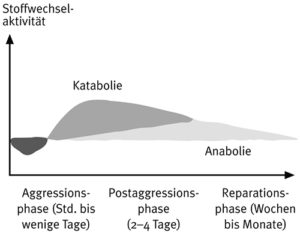
Postoperativer Stoffwechsel
Hyperglykämie
Die neuroendokrine Stressreaktion (Katecholamine, Cortisol, Glucagon) erhöht also letztlich den metabolischen Umsatz mit konsekutiver Hyperglykämie, Hyperinsulinämie, Insulinresistenz, gesteigertem Proteinabbau und negativer Stickstoffbilanz. Die Hyperglykämie ist dabei einerseits das Resultat einer gesteigerten Glykogenolyse und andererseits einer zunehmenden Glucosebildung und peripheren Glucoseverwertungsstörung. Normalerweise wird die Gluconeogenese zwar durch eine Hyperglykämie gehemmt, aber postoperativ wird die hepatische Gluconeogenese noch zusätzlich stimuliert, weil der Leber durch die Gewebeverletzung und -destruktion große Mengen an Laktat aus schlecht durchblutetem Gewebe, Glyzerol aus dem Fettgewebe und Alanin aus dem Proteinabbau angeboten werden.
Katabolismus
Die metabolische Stressreaktion induziert einen gesteigerten Proteinabbau und hemmt die Proteinsynthese, so dass direkt nach der Operation eine Nettoproteinabnahme mit negativer Stickstoffbilanz fortbesteht. Der Abbau endogener Proteine liefert durchschnittlich 25 % des Energieumsatzes, wobei nicht nur die Muskulatur des Bewegungsapparates von der Katabolie betroffen ist, sondern auch das Myokard (mit konsekutiver Dilatation der Herzkammern und verminderter Auswurfleistung) und die zirkulierenden Funktionsproteine. Der hauptsächliche Proteinabbau findet aber in der Skelettmuskulatur statt, obwohl die Verluste der Haut, des Darmes und der Lunge ebenfalls erheblich sein können. Dieser Proteinabbau wird durch Immobilisation, Fieber, Hunger und Glucokortikoide noch verstärkt.
Der Proteinabbau bezieht sich nicht nur auf viszerale Proteine, sondern auch auf die Skelett- und Herzmuskulatur, Lunge, Darm und Haut.
Anabolismus
Die Freisetzung anabol wirkender Hormone (Insulin und Wachstumshormon) wird postoperativ ebenfalls beeinflusst. Insulin wird zunächst vermindert freigesetzt und in seiner Wirkung durch die periphere Insulinresistenz beeinträchtigt, so dass der Blutglucosespiegel deutlich steigt. Im späteren Stadium wird Insulin vermehrt sezerniert, ohne allerdings seine anabolen Fähigkeiten voll entfalten zu können. Da die endogene Glucoseproduktion durch Insulin nicht gehemmt wird, findet sich weiterhin eine Hyperglykämie. Zugleich greifen wegen der peripheren Glucoseverwertungsstörung die meisten Gewebe auf die Fettoxidation als alternative Energiequelle zurück, zumal die intrazelluläre Lipolyse durch die Katecholamine angeregt wird.
Gestörter Metabolismus
Im klinischen Alltag weisen sowohl eine gestörte Glucosetoleranz und erhöhte Akute-Phase-Proteine auf eine weiterhin bestehende Stoffwechselstörung hin. Nach mittelgroßen unkomplizierten Operationen ist meistens nach zwei bis drei Tagen die katabole Phase überwunden. Bei größeren Eingriffen und insbesondere nach septischen Komplikationen dauert diese Phase bis zu mehreren Wochen.
Es mehren sich die Hinweise, dass die beschriebene Katabolie des Postaggressionsstoffwechsels keine zwangsläufige Folge des operativen Eingriffs ist, sondern dadurch hervorgerufen wird, dass ein „ausgehungerter“ Patient operiert wird. Wenn der Patient nämlich 24 Stunden vor der Operation, während der Operation und direkt nach der Operation parenteral ernährt wird, dann ist die Katabolie nicht in demselben Maße nachweisbar.